|
|
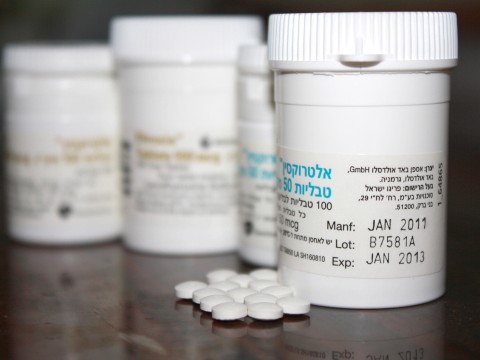
"שינוי מאוד מהותי באיכות התכשיר" [צילום: איציק וולף]
|
|
|
|
|
|
|
התפתחות דרמטית בפרשת האלטרוקסין שנחשפה לראשונה ב-News1. מסמכים פנימיים של משרד הבריאות מגלים כי למשרד ידוע על שינוי שנעשה בחומר הפעיל של התרופה אלטרוקסין המשמשת חולים הסובלים מפעילות לקויה של בלוטת התריס. זאת בניגוד לטענות הרשמיות של המשרד עד כה כי השינויים שגרמו לתופעות לוואי קשות מאוד למטופלים נעשו רק בחומרי המעטפת של התרופה.
על-פי מסמכים שחשף העיתונאי רן רזניק בעיתון ישראל היום (יום ה', 04.10.12), חברת גלקסו סמית קליין שייצרה את האלטרוקסין וחברת פריגו, המשווקת את האלטרוקסין בישראל, לא דיווחו למשרד הבריאות על השינוי בחומר הפעיל של התרופה כאשר הגישה את התרופה בהרכבה הכימי החדש לרישום בישראל. גם לאחר שהתגלו תופעות הלוואי הקשות לא נמסר כל מידע על שינוי בחומר הפעיל של האלטרוקסין. אפילו ועדת הבדיקה המיוחדת שהוקמה במשרד הבריאות בעקבות חשיפת הפרשה ב-News1 לא קיבלה כל מידע בנושא.
בחקירה שערך אגף הרוקחות במשרד הבריאות בין החודשים ינואר למאי 2011 התגלה השינוי שנעשה - החומר הפעיל שונה מחומר בעל חלקיקים קטנים לחומר בעל חלקיקים גסים.
ממסמך פנימי של בכיר במכון לביקורת חומרי רפואה באגף הרוקחות עולה כי "במהלך ההתכתבות עם היצרן התגלה שהוא שינה את החומר הפעיל - מחומר פעיל בעל גודל חלקיקים קטן לחומר פעיל בעל גודל גס של חלקיקים, ללא שדיווח למשרד הבריאות... זהו שינוי מאוד מהותי באיכות התכשיר... גודל החלקיקים יכול להשפיע על התמוססות התרופה ועל זמינות התרופה לחולה... התנהלות היצרן במהלך החידוש הייתה לא תקינה וכללה אינפורמציה חלקית, שלא לומר שגויה, ונשאלת השאלה איזו פעולה צריך לנקוט משרד הבריאות לאור התנהלות זו... הנהלת המשרד צריכה לשקול אם אפשר לנקוט צעדי עונשין נגד היצרן".
במסמך נוסף כתב אותו הבכיר באגף הרוקחות: "איני מבין למה נדרשו כמה התכתבויות עד שהחברה חשפה את המצב האמיתי... יש כמה בעיות, המרכזית שבהן היא שיש הבדל משמעותי בהתמוססות התכשיר בין הפורמולה הישנה לפורמולה החדשה, שבה גם שונה גודל החלקיקים... צריך לעשות ניסוי לבדיקה אם יש הבדל בספיגה לפני ואחרי השינוי, דבר שאולי מסביר את תופעות הלוואי".
גם לאחר שהתגלה המידע למשרד הבריאות - איש לא טרח לדווח על כך למטופלי האלטרוקסין שרבים מהם לא חזרו גם היום, יותר משנה וחצי לאחר שינוי הפורמולציה של התרופה, לאיזון הורמונלי.